心力衰竭患者更换CRTD以及术后程控管理
病例类型
完美的病例
病史资料(女,75岁,60kg)
就诊日期: 2015年9月11日。
主诉: 因“腹胀、嗝逆1月,加重伴纳差4天”入院。
现病史: 患者1月前无明显诱因腹胀、嗝逆,伴间断上腹隐痛,偶有进食后呕吐胃内容物,呕吐非喷射性,呕吐物非血性、宿食及胆汁样,不伴腹泻、畏寒、发热,未诊治。入院前4天,上述症状加重,伴纳差、乏力,于2015年9月11日来我院消化内科就诊,门诊收入我院消化内科。病程中,小便量约1000ml/天,大便正常,随眠欠佳,近期体重变化情况不详。
既往史: 间断心悸、气短10年,4年前因“扩心病”行CRTD植入,时有下肢浮肿,近月来卧位咳嗽,否认黑矇、晕厥史;否认高血压、糖尿病病史。
体格检查: 体温36.5℃、心率55bpm、呼吸20次/分、血压126/70mmHg。 神志清楚,精神差,无贫血貌,唇无发绀,高枕卧,颈静脉充盈,心界向左下扩大,心律齐,心音强弱略不等,无明显病理性杂音,腹软,剑下压痛,无反跳痛及肌紧张,肝脾肋下未满意扪及,下肢不肿,神经系统查体未见异常。
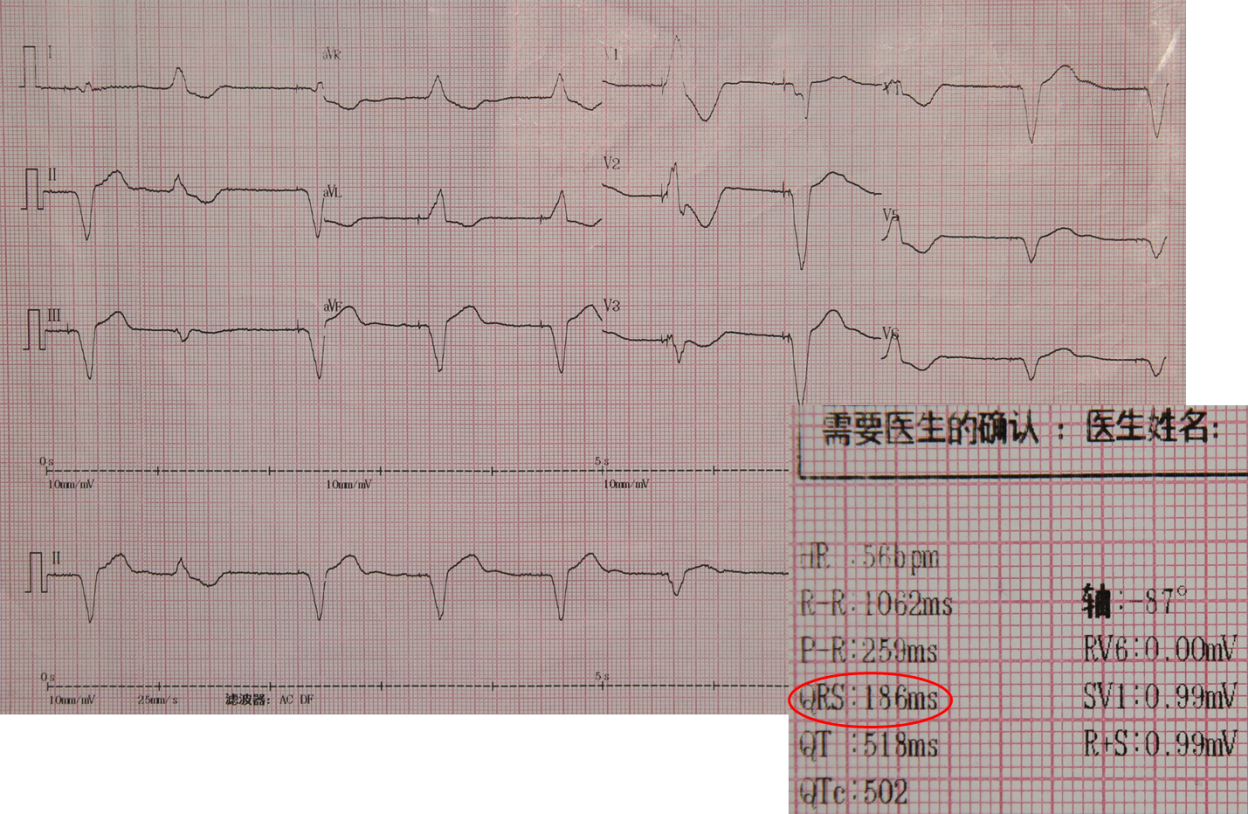
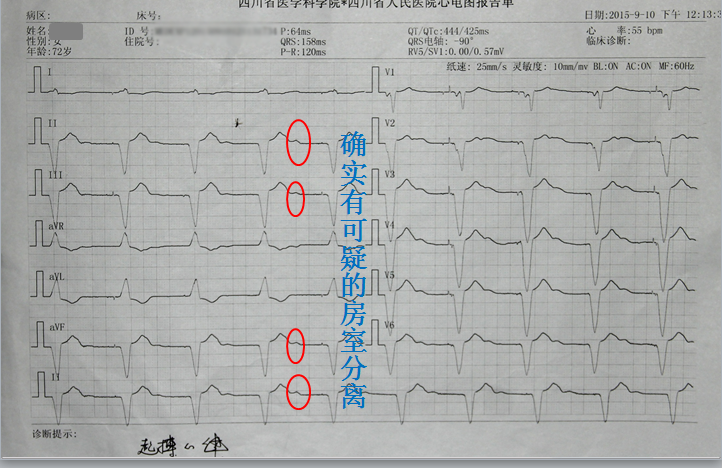
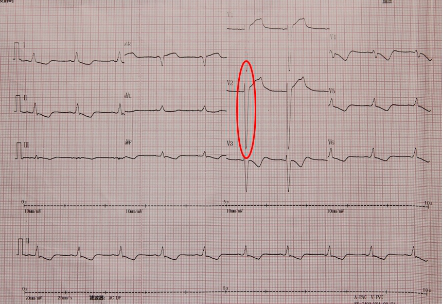
入院心电图: 起搏心律,55次/分,QRS宽度186ms,偶发室早。
超声心动图以及BNP: 全心增大,左室收缩功能轻度降低。二尖瓣重度关闭不全,三尖瓣中度关闭不全;右室收缩功能降低。主动脉硬化,主动脉瓣退变伴轻度关闭不全。心律失常。EF:0.43 RV 29 LA49×66×65 LV(D):58。 心尖段及前壁心尖段非透壁性心肌梗死,其余心肌节段血流灌注/代谢正常。
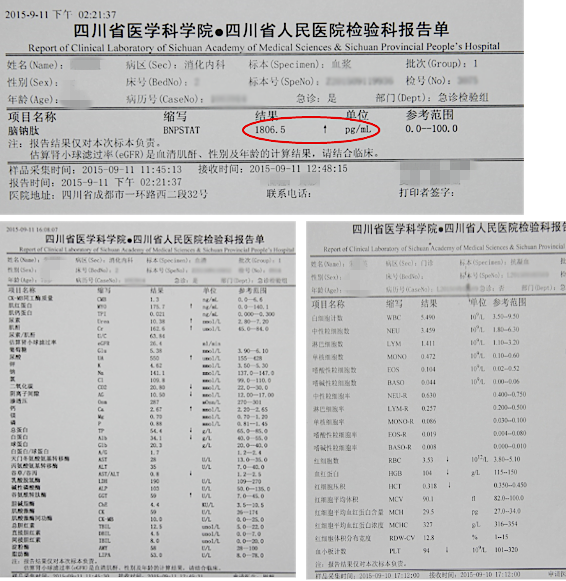
影像学检查:
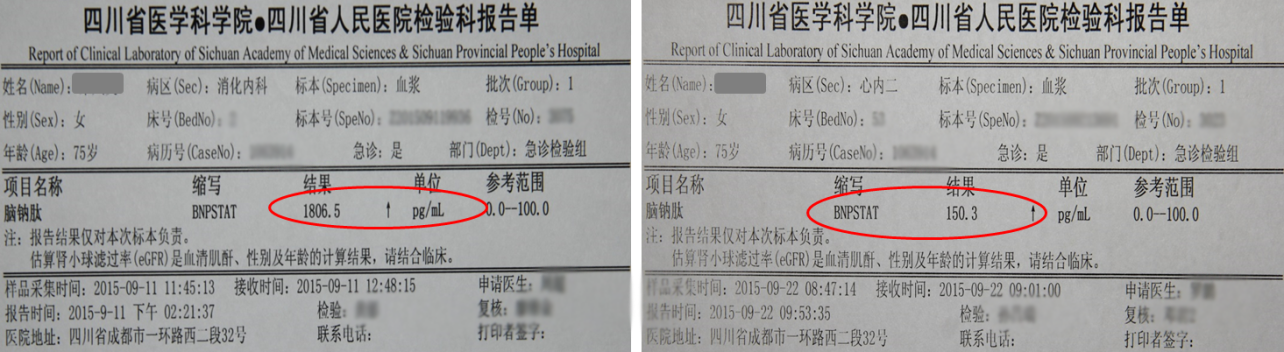
实验室检查:
初步诊断
病症: 1.腹胀、嗝逆待诊; 2.扩张型心肌病、CRTD植入术后,慢性心力衰竭。
诊治过程: 消化科医师考虑患者嗝逆为心脏起搏所致膈神经刺激(DNS),通过联系床旁起搏器调试证实为左室电极起搏所致DNS;且发现常规调低左室输出致DNS消失时,左室电极不能起搏。
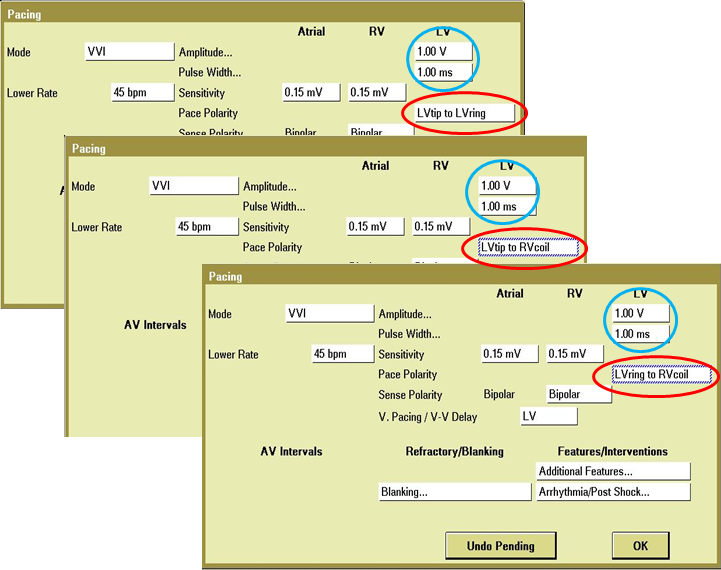
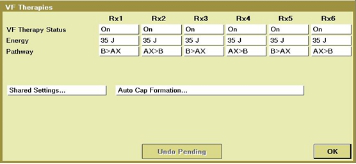
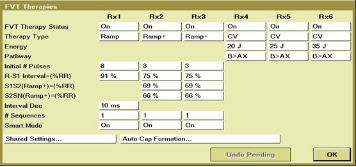
处理方法: 分别固定脉宽、电压、起搏向量,确定一个可以接受的最大脉宽;在这一脉宽和某一固定起搏向量下,找到引起DNS的最小输出电压;在上述的脉宽和电压下,寻找左室电极最佳起搏向量。通过反复调试,最后寻找到膈神经刺激阈值与左室起搏阈值间的窗口: 脉宽1.0ms、输出1.0V、起搏向量LV ring to RV coil,该参数下,病人左室起搏正常,且无DNS。
后续治疗: 通过调试,患者嗝逆消失;但是,心悸、气短、腹胀、纳差、卧位咳嗽症状缓解不明显,消化科行相关检查基本排除原发性消化系统病变,考虑为心衰所致,于2015年9月16日转入心内科(我科)进一步诊治。
转入诊断: 1. 扩张型心肌病、全心长大; 2. CRTD植入术后、起搏心律、膈神经刺激、慢性心衰急性加重。
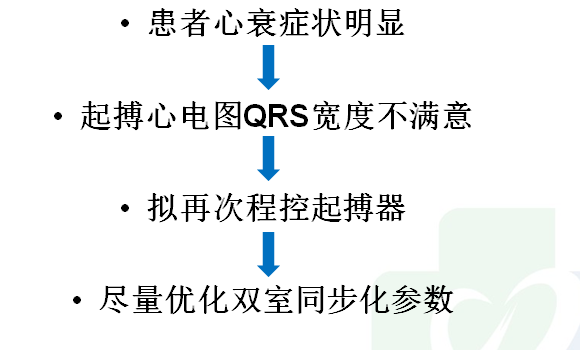
治疗思考:
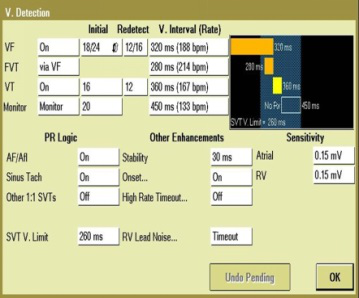
再次程控结果: 1、临近电耗竭。
2.心房电极感知丧失。
3.心房起搏不良。
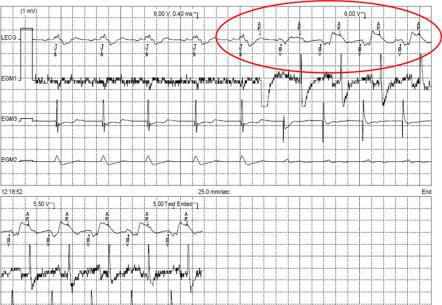
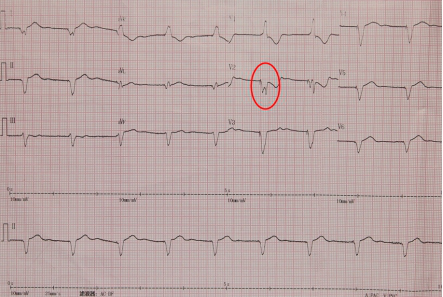
回顾心电图:
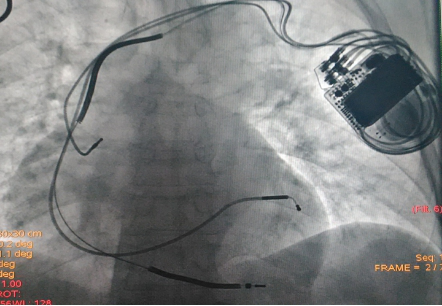
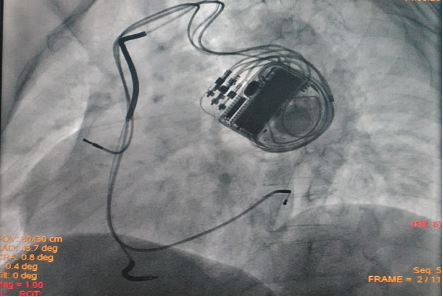
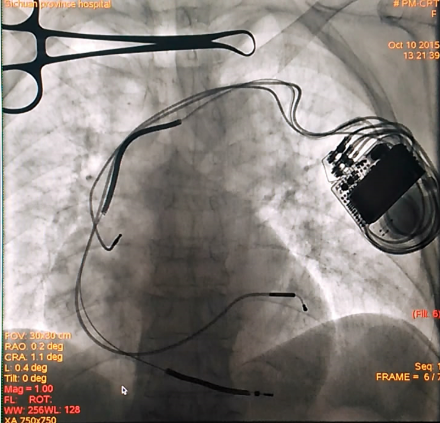
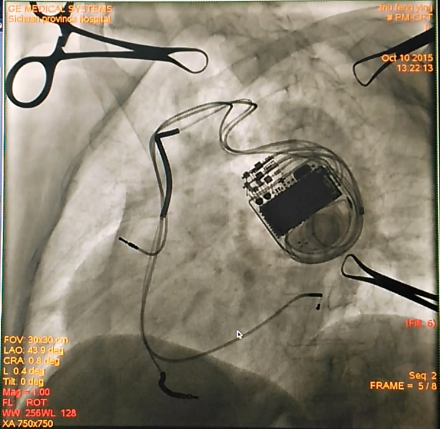
透视图: 心房电极位置未变,但是程控测试起搏感知均没有。
患者入院时真实状态: 心房起搏、感知功能丧失,起搏器以DDD工作,患者自身有房波,但起搏器感知不到,自己规律发放无效AP,并按照设定AV发放双室BiVP,且有DNS及双室同步差,导致患者入院前处于:起搏器导致的房室分离+室内同步差+明显膈神经刺激。
最佳解决方案: 1.更换心房电极+调整左室电极,解决房室分离、室内同步差、避免DNS窗口过窄问题。 2.更换起搏器,解决电耗竭问题。 但是,患者及家属认为“起搏器的植入对其帮助不大,而且贵“,不想再次手术,也不愿更换起搏器,希望医生”没电就算了,不换起搏器了,给我们用好点的药吧“。
新方法尝试: 1、DNS已经解决,首要解决房室同步问题。关闭心房电极,降低Lower rate,采用VSR模式,心室感知触发心室起搏。
2.寻找最佳的起搏模式以及LV起搏向量 1)其次寻找最佳的心室起搏模式(尽量窄QRS) VRS模式下:BiV? LV? RV? 2)LV起搏向量的选择:LV tip to LV ring?;LV tip to RV coil?; LV ring to RV coil? 选择过程:入院时为双室起搏模式(右室提前40ms)、QRS 186ms,尝试多种双室模式(分别调节左室、右室提前程度),均不能获得较窄的QRS;而VRS模式下的单LV起搏却能获得较窄的QRS。 VRS模式下单左室起搏 QRS140ms VS 双室起搏QRS160ms。
3.保留除颤功能,即使是在RV起搏功能关掉的情况下。
程控后,患者感受: 患方态度转变了!决定更换起搏器了,原因很简单:“不咳了”! “我们妈妈原来好长一段时间肚子痛和睡下去就咳,后来你们调了,先是肚子不跳了;之后,你们第二次调了起搏器的第二天,我妈睡下去就不咳了,可能调好了以后,起搏器还是起点作用的。”但患者家属觉得“现在挺好“,要求尽量简化手术避免风险,不愿更换及调整心房、左室电极。
手术过程
手术时间: 2015年10月10日。
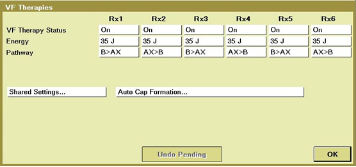
手术过程(一): 更换成D394TRG。 心房导线位置:右心耳 4574电极。 右室导线位置:心尖 6944电极。 左室导线位置:4194电极 ,侧静脉。
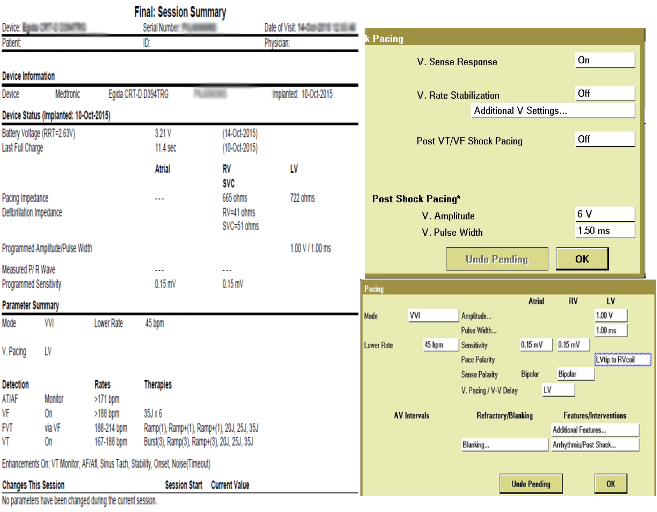
手术过程(二): 导线电学参数。
手术过程(三): 术中再次确认LV电极膈肌刺激阈值:2.0 mV,LV电极在1.0ms、LVring to RVcoil输出参数下的起搏阈值最低: 0.5V。最后选择的LV输出参数:电压1.0V、脉宽1.0ms、LVring to RVcoil。
术前术后对比
BNP指数改变:
其他说明: 起搏器调试及更换前后的用药情况。
术后情况
出院前程控参数:
术后用药: 原有药物不变。
病例总结
病例小结: 本例患者女性、79岁,基础心脏病为扩张型心肌病,4年前植入CRTD;此次因腹胀、嗝逆1月,加重伴纳差4天入消化科,病程中伴卧位咳嗽、间断呕吐。入院后经相关检查证实患者消化道症状由起搏器膈神经刺激以及心衰加重所致;进一步程控起搏器发现心房电极起搏及感知功能均丧失,由此产生起搏器相关性房室分离,成为患者心衰恶化的重要原因。结合患者同时存在起搏器电耗竭,最佳解决方案为更换心房电极、调整左室电极位置、更换起搏脉冲发生器。但患方认为起搏器对其疾病帮助不大,拒绝。在这种情况下,通过较为巧妙的程控,虽然没有更换心房电极及调整左室电极位置,仍然达到了治疗目的,且保留了起搏器除颤功能。患者症状得到明显改善,依从性提高,同意更换起搏器(D394TRG)。最后,取得了良好的临床效果。
病变特点及其解决方案: 1.心房电极感知及起搏功能丧失、导致房室分离,解决方案:关闭心房电极,采用VSR模式起搏,恢复正常房室关系。 2.双室起搏(BiVP)QRS变窄不明显(心室同步性差),解决方案:关闭右室电极常规起搏功能,采用VSR模式下右室感知触发单左室起搏,QRS变窄显著(心室同步性改善)。 3.膈神经刺激,解决方案:调节起搏输出的脉宽、电压、极性,仔细寻找避免膈神经刺激的有效起搏窗口。 4.右室电极常规起搏功能关闭后,ATP及除颤功能均得到保留。
该病例选择该器械植入的理由: 该病例采用右室感知触发左室起搏,得到良好临床效果,理应采用新一代VIVA获得更佳疗效,但该病例为更换病人,心房电极感知、起搏均失效;沟通后,患者不同意更换心房电极,所以最终更换D394TRG。
医生体会: 1.膈神经刺激的程控需要耐心,应反复寻找不同脉宽下可能存在的起搏输出窗口和除极向量。 2.VSR触发LV或双室起搏模式,可以让心室夺获的有效性脱离对感知自身P波及AV间期的依赖;在没有AV脱漏的情况下,这种模式可以做到不依赖心房电极的房室同步。 3.在某些状态下(左、右室电极植入部位的相对关系,以及左室大小等),利用自身传导的辅助起搏、产生QRS融合,可能比单纯双室起搏充分夺获心室的同步性更好。
医生对该患者后续情况的担心: 1.自身窦率太慢或出现Ⅱ度房室传导阻滞,特别是后者。 2.左室电极有效起搏和膈神经刺激间的窗口太窄,万一左室电极起搏阈值变化,两者不能兼顾。 3.VSR触发LV或双室起搏模式虽然为该患者解决了房室同步和改善了室内同步问题,但这种模式始终不能做到左室优先。
CRT/ICD疗法
Cardiac Resynchronization Therapy( CRT)是一种非药物治疗心力衰竭的方法,在右心房、右心室和左心室分别植入电极导线,通过起搏的方法使心房和左、右心室按顺序激动,以恢复心脏收缩的同步性,称为心脏再同步治疗(CRT)。
医师介绍
唐艺加,男,心血管内科,学历:医学硕士。2003年重庆医科大学心血管内科硕士研究生(研究方向:心血管介入诊疗)毕业后,于四川省人民医院工作至今;先后从事了住院医师、住院总医师、主治医师工作;于2013年~2014年通过为期1年的卫生部(现卫计委)心血管疾病介入诊疗培训(心律失常及器械植入)及相关考核、考试。对心血管疾病诊治有丰富的临床经验;擅长各种心律失常及心衰的药物及介入诊疗。作为主研者或研究者从事了多项国家级、省级科研项目。现为四川省医学会心电生理和起搏专业委员会秘书、青年委员。