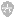S-ICD在TV-ICD移除术后患者的应用及预后:临床应用分析及与再次TV-ICD植入的对比研究
植入性心脏转复律除颤器(Implantable cardioverter- defibrillators, ICD)可有效预防心脏性猝死(sudden cardiac death, SCD)。传统的经静脉ICD(Trans-venous ICD, TV-IVD)的并发症主要集中于脉冲发生器囊袋和经静脉的导线。而皮下ICD(Subcutaneous ICD,S-ICD)是TV-ICD的一种有效的替代治疗方法。S-ICD不需要经静脉植入导线,因此适用于静脉入路存在问题或者感染高风险的患者,例如因并发症而需要移除TV-ICD的患者。本研究旨在分析对于TV-ICD移除术后的患者,S-ICD的临床应用情况,并对比移除术后植入S-ICD和再次植入单腔TV-ICD两种不同治疗策略的预后。
该研究回顾性分析了2011至2017年间在12个意大利医疗中心行TV-ICD移除术且再次植入ICD的患者(n=229),分为植入S-ICD(n=90)和再次植入单腔TV-ICD(n=139)两组,随访平均时间17个月。研究终点为植入器械和/或植入操作相关的并发症,其中严重并发症包括导致住院时间延长或需要手术干预的不良事件,非严重并发症包括无需手术干预或住院的不良事件。
植入性心脏转复律除颤器(Implantable cardioverter- defibrillators, ICD)可有效预防心脏性猝死(sudden cardiac death, SCD)。传统的经静脉ICD(Trans-venous ICD, TV-IVD)的并发症主要集中于脉冲发生器囊袋和经静脉的导线。而皮下ICD(Subcutaneous ICD,S-ICD)是TV-ICD的一种有效的替代治疗方法。S-ICD不需要经静脉植入导线,因此适用于静脉入路存在问题或者感染高风险的患者,例如因并发症而需要移除TV-ICD的患者。本研究旨在分析对于TV-ICD移除术后的患者,S-ICD的临床应用情况,并对比移除术后植入S-ICD和再次植入单腔TV-ICD两种不同治疗策略的预后。
TV-ICD移除术的主要原因是感染(SICD组vs. TV-ICD组:73% vs. 52%,p<0.001=,其次为导线故障、症状性静脉血栓形成或静脉阻塞(见图2)。在S-ICD植入患者中,所有患者至少有1个向量通过所有体位的体表心电图筛查,71位(79%)至少有2个向量通过筛查,17位(19%)3个向量均通过筛查。43位(47%)S-ICD患者的囊袋为标准的皮下囊袋,其他57位(53%)为肌肉下或者肌间囊袋。71位(78%)S-ICD患者术中进行除颤阈值测试,均除颤成功。从临床特征上分析,S-ICD组患者平均年龄更小(53岁 vs.60岁, p=0.011),男性更多。两组在基础心血管疾病,心功能和合并症方面无明显差异(见表1)。2011年TV-ICD移除术后S-ICD的植入比例为9%,2017年增加至85%(见图1)。
表1. 患者临床特征分析
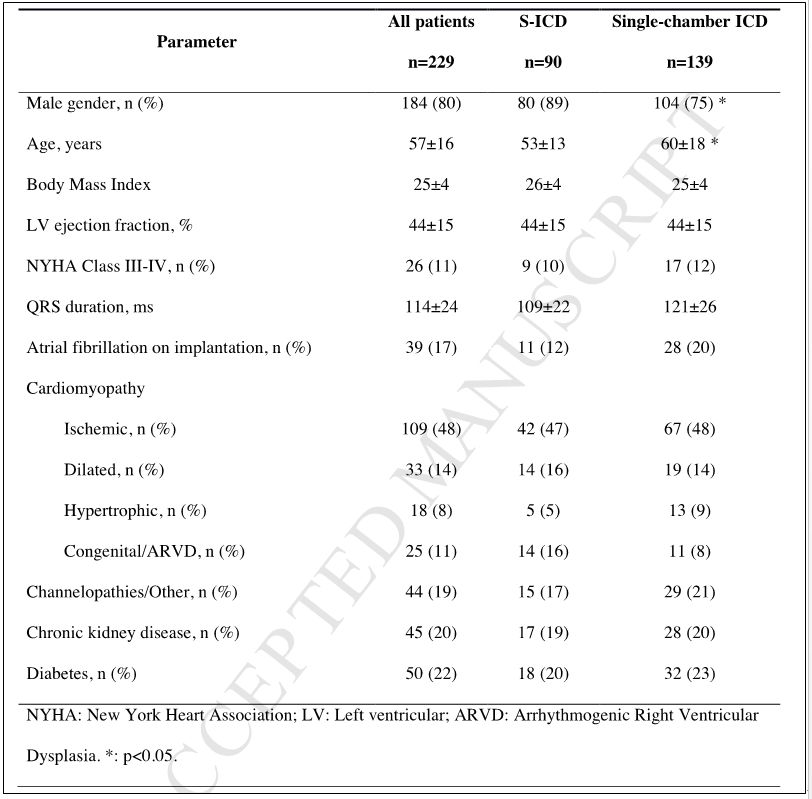
表2. TV-ICD移除术后患者选择S-ICD的原因分析

图1. S-ICD应用情况和TV-ICD移除情况分析
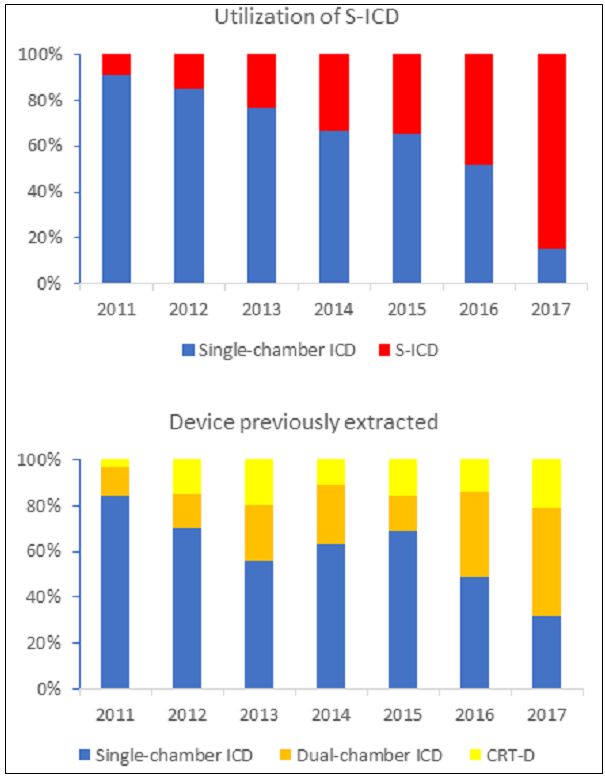
图2. ICD移除原因和类型分析(S-ICD植入组vs. 再次单腔TV-ICD植入组)
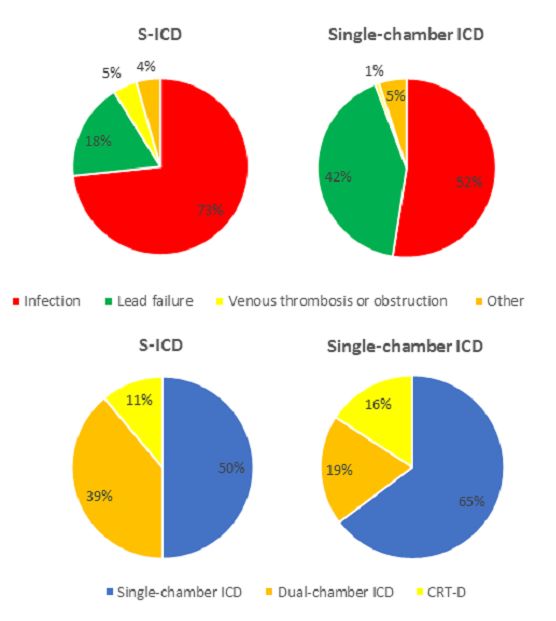
随访期间共有15位(6.5%)患者死亡(S-ICD组4例,TV-ICD组11例),1位患者进行心脏移植,无患者死于SCD。随访期间共记录25例严重并发症(见表3),14例非严重并发症(见表4)。并发症的发生率两组间无统计学差异 (HR: 0.94, 95% CI: 0.49-1.92, P=0.94)。S-ICD组无导线故障、感染或植入器械相关的死亡。在再次植入TV-ICD组,共发生1例导线断裂,2例植入器械相关感染,其中1例死亡。研究发现,脉冲发生器埋置在肌肉下或肌间的S-ICD患者并发症发生率显著降低(HR:0.21,95% CI:0.05-0.87,p=0.048)。
表3. 随访期间主要并发症
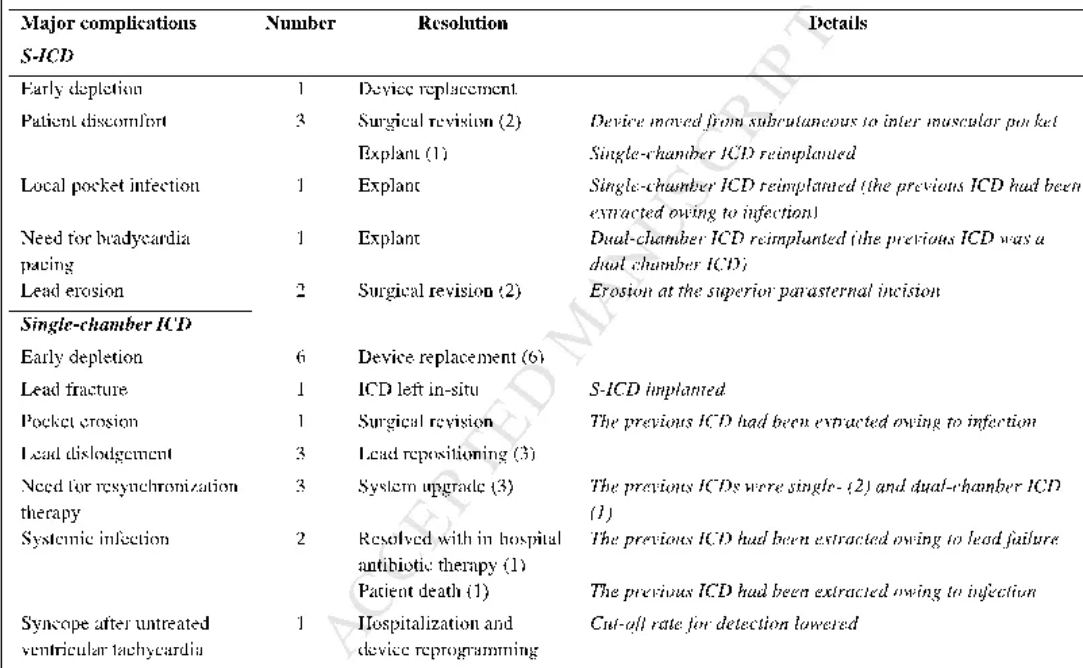
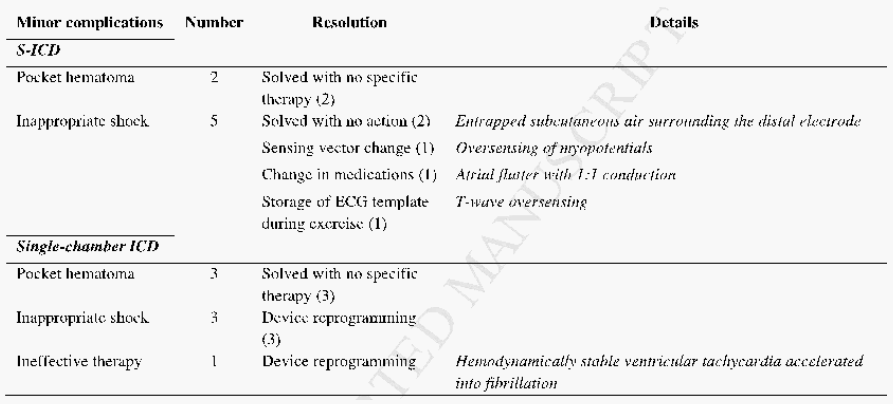
表4. 随访期间非主要并发症

据悉,该研究是首个关于TV-ICD移除术后患者进行S-ICD或再次单腔TV-ICD植入治疗的对比研究。研究结果提示,在TV-ICD移除术后的患者,S-ICD的应用逐年增加,S-ICD尤其适用于年轻的、由于感染原因行TV-ICD移除的患者。TV-ICD移除术后,S-ICD和再次单腔TV-ICD植入的并发症发生率组间无显著差异。S-ICD的脉冲发生器埋置于肌肉下或肌间时,并发症发生率可进一步降低。
本文摘译自:Heart Rhythm (2018), doi: https://doi.org/10.1016/ j.hrthm. 2018.10.026).