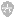起搏动态|闫丽荣:体质指数对全皮下植入式心律转复除颤器安全性和有效性的影响研究
全皮下植入式心律转复除颤器(subcutaneous implantable cardioverter-defibrillator,S-ICD)已经证实可用于室性心律失常高危患者。试验模型研究显示肥胖增加经静脉除颤系统的除颤阈值(DFT)。肥胖还会增加介入相关并发症风险。此外,低体重会增加S-ICD患者侧方囊袋的不适感和破损风险。故该研究假设肥胖会增加恰当电击失败风险,体重异常(低体重或肥胖)会增加S-ICD手术相关并发症风险。
研究方法:
1、研究人群和除颤测试。研究人群为IDE(Investigational Drug Exemption)研究中植入S-ICD患者,该研究为前瞻性、非随机、多中心试验,入选无需起搏或ATP治疗有ICD适应证的成年患者。S-ICD植入采用标准手术操作流程,术中进行急性期除颤测试。采用经胸50Hz直流电诱发心室颤动(VF),S-ICD自动识别VF,并给予65J电击除颤。主要有效性终点是成功转复诱发的VF,即在任一除颤向量下65J连续2次成功转复。慢性期除颤测试在术后至少150天后进行,同样重复上述除颤试验过程。
2、临床随访及研究终点。术后电除颤能量设为80J。S-ICD术后1个月,3个月,6个月及之后每6个月均进行随访,至研究结束。如患者发生自发性电击或病情变化,则及时进行评价。每次随访均进行S-ICD程控检查。首次电击失败定义为:急性期除颤测试(65J)、慢性期除颤测试(65J)或自发性室性心律失常事件(80J)中任何首次电击未能转复VF或室速。除颤阻抗在急性期除颤测试中进行评价。并发症分为3类:感染相关并发症(囊袋破损,切口延时愈合,表皮和全身感染),位置不恰当相关并发症(S-ICD装置不适感、脉冲发生器或导线位置不理想),不恰当电击。
3、统计分析。按照美国疾病控制和预防中心标准根据体质指数(BMI)对患者进行分层:低体重(BMI<18.5 kg/m2),正常体重(18.5 kg/m2≤BMI≤24.9 kg/m2),超重(25.0 kg/m2≤BMI≤29.9 kg/m2),肥胖(BMI≥30.0 kg/m2);低体重患者数量较少,故与体重正常患者归为一组进行统计学分析。
研究结果:
BMI及其他基线特征。共纳入321例植入S-ICD患者(BMI分布见图1),低体重患者8例(2.5%),正常体重患者71例(22.1%),超重患者105例(32.7%),肥胖患者137例(42.7%)。与正常和低体重组患者相比,超重组和肥胖组患者年龄较大,男性比例较多,血肌酐水平较高,合并糖尿病、高血压、房颤、心力衰竭等并发症比例较高,以及利尿剂、抗凝、降糖等合并用药较多(详见表1)。
图1. 患者体质指数(BMI)分布情况
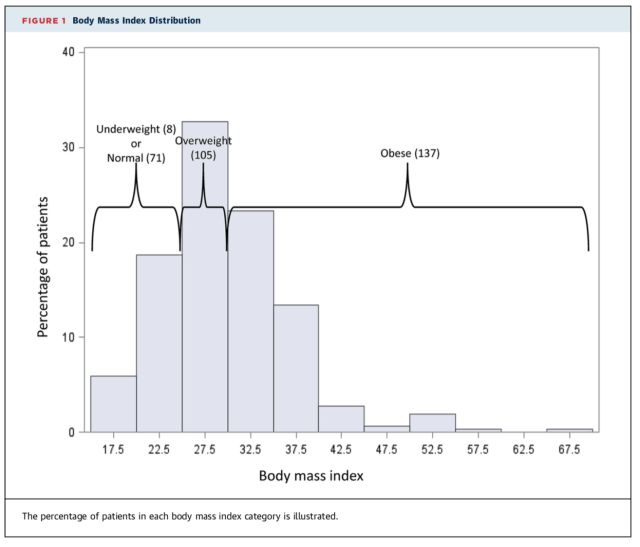
表1. 按体质指数(BMI)分组比较患者基线特征
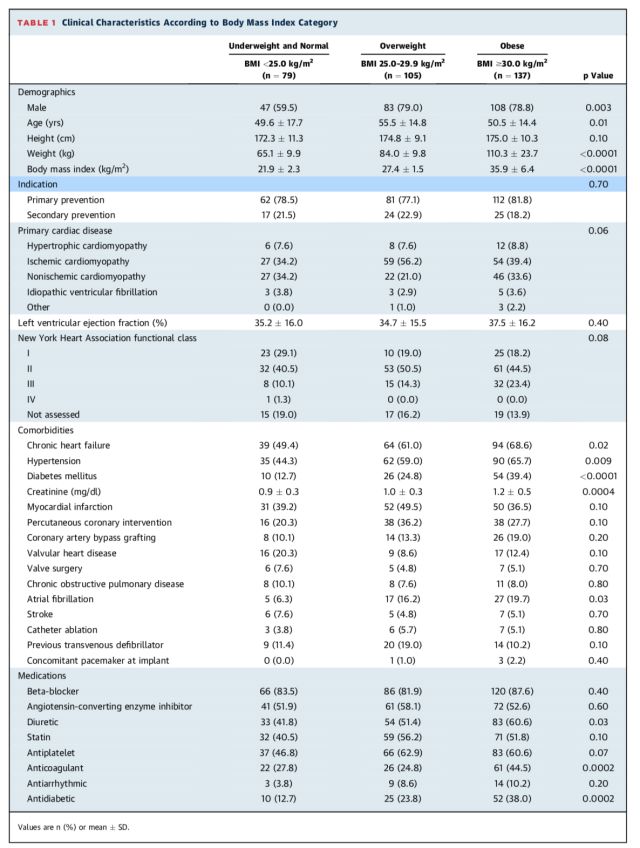
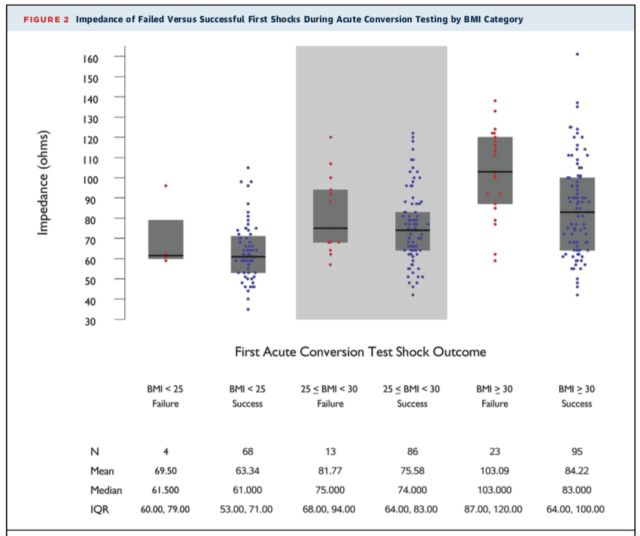
首次电击失败率。52例患者首次电击失败,其中41例发生于急性期除颤测试,11例发生于慢性期除颤测试,5例发生于自发性室性心律失常事件。急性期除颤测试:首次电击失败率随着BMI分层升高而升高(P=0.04),见表2。肥胖患者急性期除颤测试中,首次电击失败患者的除颤阻抗高于首次电击成功患者(103.5Ω vs. 84.6Ω,P=0.001),见图2;体重正常组和超重组未观察到上述除颤阻抗变化。除颤阻抗在首次电击和第二次电击中具有良好的一致性(R2 = 0.98)。41例急性期除颤测试首次电击失败患者中,24例患者经过再次除颤测试成功完成手术,未进行导线或脉冲发生器重置;2例患者(均为肥胖患者)尽管除颤测试失败仍植入S-ICD,未尝试重置导线或脉冲发生器位置;15例患者重置导线或脉冲发生器位置,其中8例患者(3例超重患者和5例肥胖患者)重置后除颤测试成功完成,除颤阻抗平均由81Ω降至77Ω。其余7例患者重置后除颤阻抗平均由107Ω降至92Ω,但除颤测试仍失败,6例患者移除S-ICD系统(均为肥胖患者),1例患者经70J两次电击成功故保留S-ICD系统。41例急性期除颤测试首次电击失败的患者中,随访期4例患者发生自发性室性心律失常事件,3例患者80J电击成功终止,1例患者(正常体重)第五次电击成功终止。
表2. 体质指数(BMI)分组间S-ICD除颤有效性比较
图2. 各体质指数(BMI)分组中急性期除颤测试首次电击成功患者与失败患者的除颤阻抗比较
慢性期除颤测试:80例患者进行慢性期除颤测试,各BMI组间首次电击失败率无统计学差异(P=0.40),见表2。11例患者首次电击失败,其中4例患者曾在急性期测除颤测试中首次电击失败。
随访720天,各BMI组间生存率相似(正常和低体重患者96.1%,超重患者95.8%,肥胖患者98.4%,P=0.90)。4例正常和低体重患者发生11次自发性室性心律失常事件,8例超重患者发生16次事件,13例肥胖患者发生24次事件。各BMI组间80J首次电击失败率无统计学差异(P=0.60),见表2。5例患者80J首次电击失败,其中仅有1例为急性期测除颤测试中65J首次电击失败患者,在随后的两次诱颤中65J电击均成功转复,故该例正常体重患者没有重置导线或脉冲发生器位置。
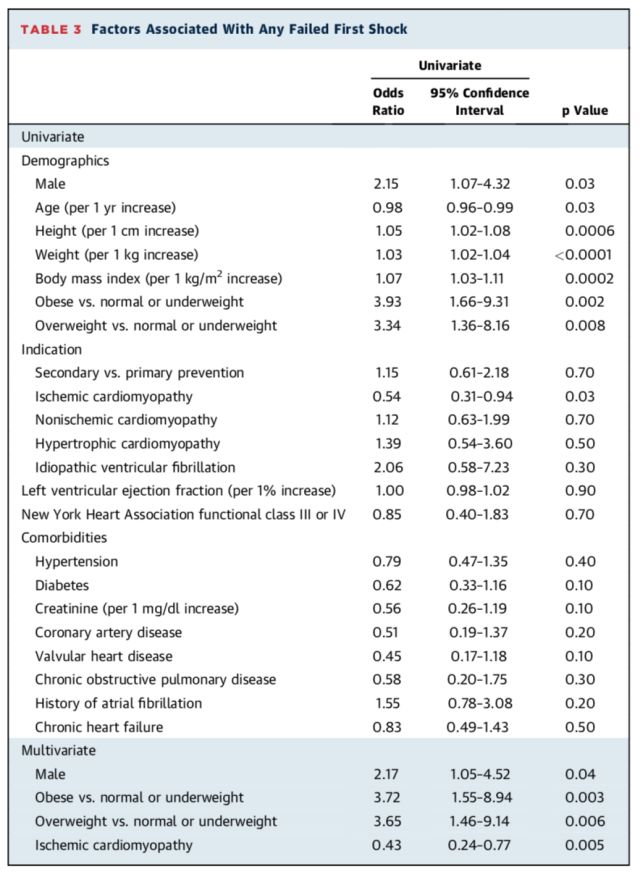
任何首次电击失败发生率随BMI分层升高而升高(正常和低体重患者6.3%,超重患者18.1%,肥胖患者20.6%,P=0.02)。8例低体重患者无任何首次电击失败发生。多因素Logistic回归分析显示:男性,缺血性心肌病和BMI与任何首次电击失败发生率独立相关,详见表3。与正常和低体重患者相比,超重患者首次电击失败发生相对风险(OR)为3.65(95%CI 1.46-9.14,P=0.006),肥胖患者OR为3.72(95%CI 1.55-8.94,P=0.003)。
表3. 任何首次电击失败影响因素分析
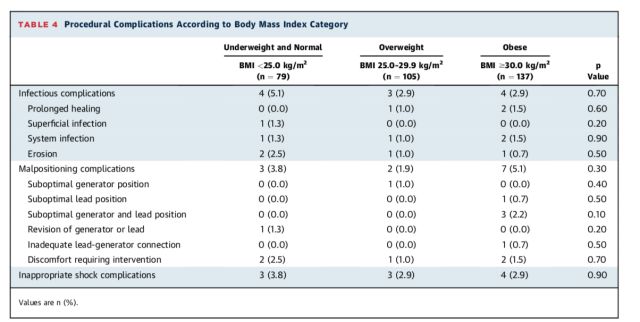
并发症:各BMI组间感染相关、位置不恰当相关及不恰当电击等并发症发生率均无统计学差异(P均>0.05),详见表4。8例低体重患者未发生任何并发症。Logistic回归分析未发现感染及位置不恰当相关并发症的预测因素。房颤病史增加不恰当电击风险(OR3.9,95%CI:1.07-14.52,P=0.04)。
表4. 各BMI分组手术相关并发症发生率比较
该研究有一定的局限性。IDE研究中仅有8例低体重患者;未精确测试急性期DFT;慢性期除颤测试和自发性心律失常事件患者数量均较少;IDE研究中未对患者生活质量进行评价;虽然肥胖与首次电击失败相关,但其中不排除有未评价的混杂因素,如右心室内径等;最重要的是,研究未能对肥胖增加首次电击失败风险的机制进行分析。但该研究结果有重要意义。如能通过优化植入技术可以改善高DFT,则肥胖患者将尤其获益;否则,肥胖患者选择ICD类型时应慎重考虑。但因缺少经静脉ICD对照,很难判定哪种ICD更适合肥胖患者。目前正在进行的TLAS S-ICD和PRAETORIAN研究对经静脉ICD和S-ICD进行随机对照,结果值得期待。
结论:肥胖增加S-ICD患者急性期除颤测试首次电击失败风险,而这一情况能否通过优化植入技术得到改善尚需进一步研究。肥胖和低体重未增加并发症发生率。
(文章摘译自:Impact of Body Mass Index on Safety and Efficacy of the Subcutaneous Implantable Cardioverter-Defibrillator JACC: Clinical Electrophysiology. 2018. DOI:10.1016/j.jacep.2017.11.019. )